生物学的同等性試験
臨床研究にいて、以下のような比較試験が行われます。
① 生物学的同等性試験⇒後発品 vs 先発品
② 優越性試験⇒医薬品 vs プラセボ
③ 非劣性試験(実際に使用されている治療薬と比較して劣ってないことを確認する試験)
⇒医薬品(試験薬) vs 医薬品(対照薬)
生物学的同等性試験(ニューロタン(50) vs ロサルタンK(50)「科研」)
【方法】
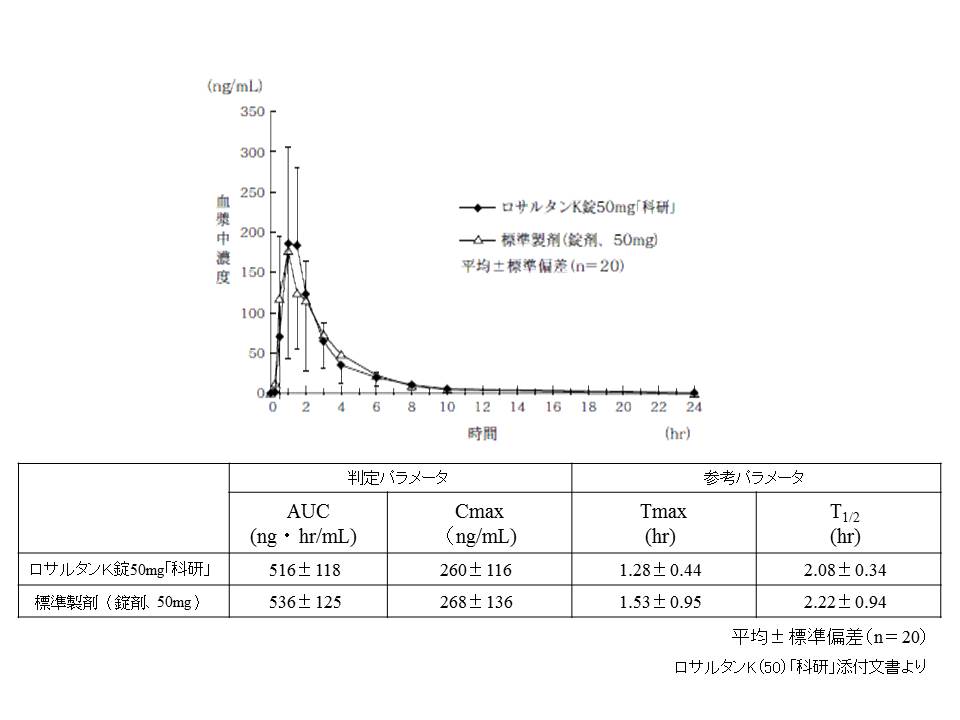
健康成人男子にロサルタンK50mg「科研」と標準製剤のそれぞれ1錠(ロサルタンとして50mg)を、絶食単回傾向投与して
血漿中ロサルタン濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、
log(0.80)~log(1.25)の範囲内であり、両剤の生物学的同等性が確認された(クロスオーバー法)。
(ロサルタンK(50)「科研」の添付文書より)
クロスオーバー法とは、2群に無作為割付を行い、あるグループには、先発品→後発品を服用し、もう一方のグループでは後発品→先発品と服用して効果をみる試験方法をいいます。生物学同等性試験のガイドラインにクロスオーバー法が記載されています。
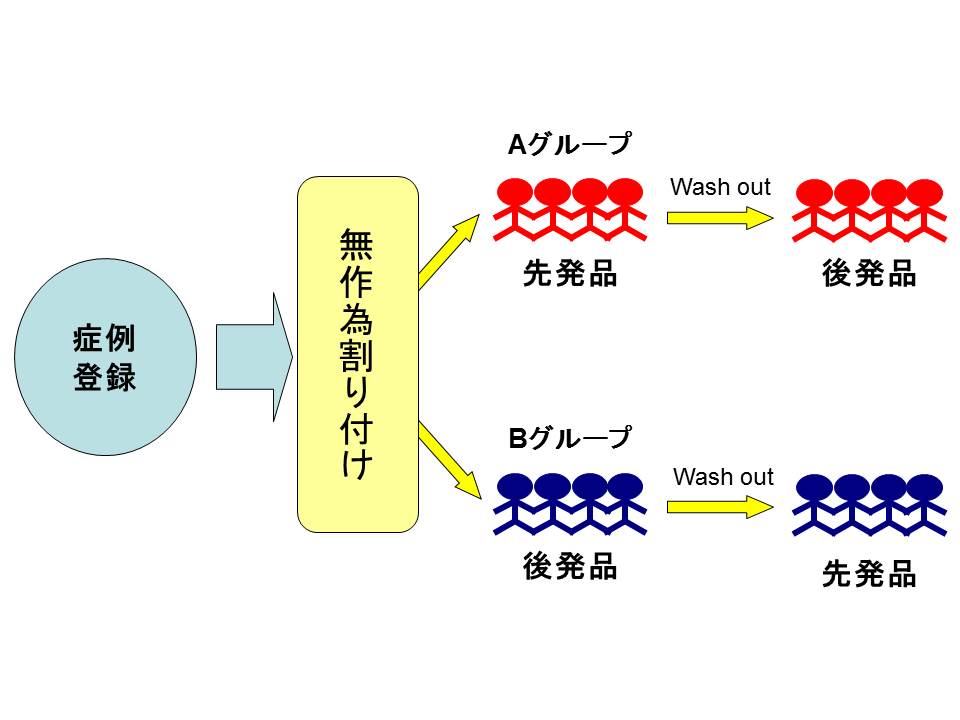
メリットとして、症例自身が対照となるため平行群間試験に比べて総症例数が少なく、ばらつきが少ないことが挙げられます。
デメリットとしては、先発品と後発品を服用する間に薬の持ち越し効果があることが挙げられます。そのため、ウォッシュアウト期間が必要となります。
2群間の同等性をp値で評価できるか?
2群間でAUC、Cmaxの平均値について、t検定を行いp値で評価を行う。
p値とは、結果の差が偶然によって生じたと考えられる確率のことをいいます。通常p値は5%未満なら有意差があると判断しますが、p値が小さいほど差があることが確実であることを示し、p値が小さいほど差が大きいことを示すわけではありません。
【結果】
① p≧0.05で「有意な差がなし」と判定された場合
有意差がないことが示されただけであって、真に差がないことを証明した訳ではありません。
p値は症例数やデータのバラツキに影響を受けやすいため、有意差がないのは症例数が足りていない場合があり、臨床試験のデザインが悪いことを示唆しているとも考えられます。
② p<0.05で「有意な差があり」と判定された場合
p値が小さいほど「差があること」が確実になったことを示している。2群に違いがないという仮説の検証の指標であり、臨床的な意義をあらわさない。症例数が多くなれば、p値は小さくなります。
したがって、p値の大きさではグループ間の差の程度を判断することが不可能であるため、p値のみで生物学同等性を議論できません。グループ間の差の程度を知るためには信頼区間(confidence interval)によって判断します。
生物学的同等性試験の臨床的な基準
先発医薬品のバイオアベイラビリティの80%に満たない又は125%を越える後発医薬品が市場に出回らないようにするため、臨床的基準を設けています。対数を加味しているために80~125%と対称的な数値となります。
90%信頼区間法にて統計解析を行い、log(0.80)~log(1.25)の範囲内にある必要があります。
logを使用する理由
正規分布しているか非正規分布しているかで統計解析の方法が変わってきます。生物学的同等性試験の統計解析はt検定で行うため、データが正規分布である必要があります。
薬学で扱うデータ(AUC、Cmaxなど)はそのままでは正規分布にならず、対数変換を行うことで正規分布となることが多い。そのため、生物学的同等性試験では原則的に対数正規分布を使用しています。
信頼区間(CI:confiidence interval)とは?
p値では、2群間の差の程度がどれくらいあるか判断できませんが、この差の程度を信頼区間(CI:confiidence interval)によって求めることができます。
90%信頼区間とは、100回繰り返した場合、母集団の推定値が90回分布する幅をいいます。見方を変えると10%はこの区間から外れて分布することになります。
一般に信頼区間は症例数(N)と関連していて、Nが増えると、信頼区間の幅は狭くなり、Nが少なくなると信頼区間の幅は広くなります。